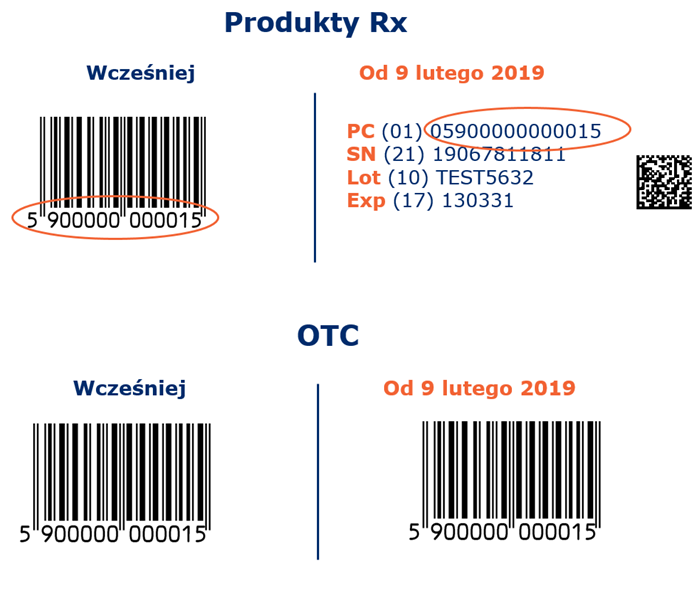
W związku z obowiązującymi wymogami prawnymi wszystkie szpitale muszą być przygotowane na skanowanie kodów kreskowych GS1 DataMatrix z produktów leczniczych, które podlegają obowiązkowi serializacji. Termin implementacji zmian organizacyjnych i techniczno-technologicznych upłynął 9 lutego 2019 r.
Jaki jest cel skanowania kodów?
Celem skanowania powinna być weryfikacja i wycofanie tzw. niepowtarzalnego identyfikatora. Należy jednak pamiętać o tym, że kod kreskowy leku może być skanowany wielokrotnie dla innych celów: automatycznej rejestracji przyjęcia dostawy, kompletacji / wydania leków na oddział, czy wreszcie potwierdzenia podania leku pacjentowi.